

近日,我院董廖斌课题组联合南京大学梁勇课题组,在国际顶级期刊 Nature Chemistry 发表重要研究成果,论文题为“ Exploring bacterial cytochrome P450s for selective activation of aliphatic C–H bonds in pentacyclic triterpenoids ”。该研究突破了五环三萜天然药物研发长期局限于少数活性位点重复修饰的瓶颈,首次实现了五环三萜B/D环惰性位点的精准活化与克级制备,将长期被视为“结构盲区”的B/D环转化为可持续利用的新修饰位点,为五环三萜创新药物研发开辟了新路径。我校中药学院2022级博士研究生张晓维与南京大学化学化工学院陈红威特任副研究员为论文共同第一作者,董廖斌教授、梁勇教授为共同通讯作者,中国药科大学为第一通讯单位。
五环三萜是一类结构多样、生物活性显著的天然产物,具备发展为类似甾体类重磅药物的结构基础,代表性分子包括HIV抑制剂贝韦立马、治疗Friedreich共济失调的奥马索隆以及Nrf2激活剂甲基巴多索隆(CDDO-Me)等。然而,长期以来,该类分子的药物开发主要依赖C-3、C-28等少数活性位点的重复修饰,难以从根本上突破临床毒副作用等关键瓶颈。与此同时,五环三萜骨架中仍存在大量未被开发的惰性C–H键位点,尤其是B环和D环区域,可能蕴藏着重塑分子活性、安全性和代谢性质的重要空间。由于现有化学与生物方法均难以对这些位点实施高效精准改造,其长期处于新药研发的“结构盲区”。因此,发展能够选择性活化五环三萜惰性位点的新型酶学工具,对于拓展其结构修饰边界和提升成药潜力具有重要意义。
细胞色素P450酶因具有精密的底物识别与催化能力,被认为是实现惰性C–H键精准活化的理想工具。但此前可作用于五环三萜的P450酶均来自真核生物,受膜结合特性限制,普遍存在异源表达困难、应用受限等问题。为此,研究团队创新性地发展了“萜类合酶-P450”定向挖掘策略,以细菌萜类合酶为锚点挖掘邻近P450酶,结合高效体外筛选平台,成功从Amycolatopsis pretoriensis中发现首个原核来源的五环三萜修饰P450酶——ApPT(CYP161H12)。该酶通过1,5-氢原子转移机制,实现了B环C-7β和D环C-15α位点的高效、高选择性活化,总收率达99%,突破了化学方法难以实现的无导向基团、高立体选择性C–H键官能化难题,并实现克级制备。机制研究进一步揭示了酶促1,5-氢原子转移介导的C7-to-C15接力氧化规律,拓展了生物催化自由基化学的研究边界。在此基础上,团队通过“化学-酶”法合成获得了一系列具有抗肿瘤、抗炎活性的迈克尔受体分子,其中部分B环新颖衍生物展现出良好的先导药物开发潜力。
该研究得到了国家重点研发计划,国家自然科学基金、江苏省自然科学基金等项目的资助。
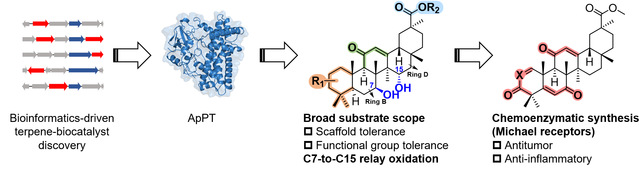 细菌P450突破五环三萜“结构盲区”,拓展天然药物开发新空间
细菌P450突破五环三萜“结构盲区”,拓展天然药物开发新空间
文章链接:https://www.nature.com/articles/s41557-026-02106-9
CopyRight CPU ZHONGYAOXUEYUAN [ 中国药科大学中药学院主页] All Rights Reserved
地址:江苏省南京市江宁区中国药科大学中药学院